2.3. Mecanismos de reacción y molecularidad
TIPOS Y MECANISMOS DE REACCIÓN
Una ecuación balanceada indica la cantidad de moles de reactivos que reaccionan y la cantidad de moles de productos que se forman, pero no nos dice cómo se lleva a cabo la reacción en sí. Existen reacciones que se producen en un solo paso, directamente, pero hay otras que son una sucesión de reacciones simples. Conocer el número de pasos en que transcurre una reacción se conoce como el mecanismo de la reacción.
Para entenderlo mejor, imaginemos que viajaremos de Lima a Buenos Aires por avión. Puede ser que el viaje se produzca directamente, es decir, que el avión vaya sin escalas hasta Buenos Aires. Pero supongamos que el avión hace una escala en La Paz, Bolivia. Nuestro viaje, entonces, ocurriría en dos pasos: Lima – La Paz, y La Paz – Buenos Aires. En ambos casos el resultado es el mismo, estaremos en Buenos Aires, pero de maneras diferentes: directamente (un solo paso) o con escalas (más de un paso).
Reacciones sencillas o elementales
Son aquellas reacciones que ocurren en una sola etapa, es decir, los reactivos chocan entre sí formando los productos. Un ejemplo de una reacción elemental es la reacción del óxido nitroso (NO) con ozono (O3):
NO(g) + O3(g) → NO2(g) + O2(g)
Podemos representar el proceso según el siguiente esquema: las moléculas de óxido nitroso y ozono chocan entre sí, dando directamente lugar a los productos.

Reacciones complejas
Son aquellas que transcurren en más de un paso. Casi todas las reacciones químicas transcurren de esta forma: en más de un paso. En todo caso, la ecuación química global está dada por la suma de las etapas elementales. Consideremos la reacción entre el óxido nítrico (NO2) y monóxido de carbono (CO):
NO2(g) + CO(g) → NO(g) + CO2(g)
Esta reacción transcurre en dos etapas:
Etapa 1: NO2(g) + NO2(g) → NO(g) + NO3(g) ETAPA LENTA
Etapa 2: NO3(g) + CO(g) → NO2(g) + CO2(g) ETAPA RÁPIDA
Global: NO2(g) + CO(g) → NO(g) + CO2(g)
Observa que la suma de las dos etapas nos da la reacción global: la estequiometria no se ve afectada, lo único que es importante en este caso es que tal reacción ocurre en dos pasos, y no por un choque directo entre el óxido nítrico y el monóxido de carbono.
Vemos en nuestro proceso que el NO3 aparece en la primera reacción como un producto y en la segunda como un reactivo, es decir: participa en el mecanismo de la reacción, pero no aparece en la ecuación global. A estas especies se les denomina intermedios (o intermediarios) de reacción.
Por lo general, una de las etapas es mucho más lenta que las otras. Por tanto, es sobre esta etapa donde se realizan los estudios de velocidades de reacción. Para determinar cuál etapa es más lenta, se necesita hacer experimentos en el laboratorio, midiendo las concentraciones a diversos tiempos. ¿Cómo podemos entender que haya una etapa más lenta, y que de ella dependa la velocidad de la reacción? Analicemos el siguiente ejemplo: supón que tienes que viajar desde la PUCP hasta el Jockey Plaza, viajando a través de la avenida Javier Prado. En esta avenida hay un semáforo en el cruce con la av. Petit Thouars que tarda bastante y que ocasiona atascos. Da igual en qué vehículo vayamos: el tiempo que tardemos en llegar a nuestro destino depende de lo que tardemos en este cruce, ya que llegar hasta aquí es más o menos fluido y a partir de este cruce también encontramos un ritmo normal. Por tanto, el tiempo que tardemos en llegar a nuestro destino dependerá de cuánto tiempo tardemos en este cruce.
MOLECULARIDAD
La molecularidad de una reacción es el número de moléculas que reaccionan en una etapa elemental. De esta manera, podemos tener:
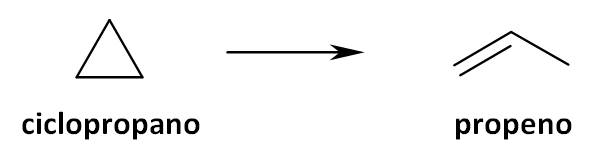
- Reacciones unimoleculares: en las que sólo participa una molécula. Un ejemplo es la conversión del ciclopropano en propeno: una molécula de ciclopropano se convierte directamente en propeno, sin necesidad de otro reactivo.
- Reacciones bimoleculares: participan dos moléculas. Constituyen el mayor ejemplo de reacciones. Todas las analizadas para los óxidos nitroso (NO) y nítrico (NO2) en el tema anterior, constituyen ejemplos de reacciones bimoleculares.
- Reacciones trimoleculares (o termoleculares): participan tres moléculas. Son menos probables, dado que requiere que colisionen tres moléculas al mismo tiempo. La formación de ozono (O3) a partir de oxígeno (O2) es un ejemplo de una reacción termolecular.
3 O2(g) → 2 O3(g)
